イオン液体(ionic liquids; ILs)は古典的な溶融塩の低融点アナログと考えられ,一般に水の沸点以 下の温度で液体であると定義される1)。この性質はイオンサイズの大きさと柔軟な形態に起因する熱 力学的な有利さに由来している。ILs は蒸気圧を示さないことや優れた熱安定性などの特異的な性質 により,過去十数年にわたって注目を集めてきた。このことから,ILs は様々な有機反応や化学プロ セスおよび抽出の分野で,揮発性有機溶媒代替物として利用されてきている。ILs の他の重要な優位 性は多様な構造と化学組成であり,種々の有機カチオンと多種類の有機あるいは無機アニオンの組み 合わせから構築できる(図 1)。最も一般的な IL カチオンはアンモニウム,ホスホニウム,ピリジニ ウム,イミダゾリウムなどである。すなわち,イオン対の多様性により,ILs は制御された化学およ び物理的性質や特異的な機能を示し,触媒や電気化学などの実用的な分野において,種々の応用が見 いだされている2)。また,このような ILs の古典的な応用を超えて,ILs の生体高分子に対する特異的 な親和性を利用して,ILs の研究対象は多糖など生体高分子関連にまで広がっている3)。さらに近年, ILs の特異的な光機能も報告されている。本報において著者は,重合性 ILs のラジカル重合を利用し た光機能性イオン液体に関する最新の研究展開について概説する。
ポリ(イオン液体)[poly(ionic liquid)s; PILs](あるいは高分子化イオン液体や高分子イオン液体と も呼ばれる)は繰り返し単位中の IL 部位が高分子主鎖を介して繋がった高分子化合物と定義され, 重合基を有する ILs の重合で得ることができる4)。このような ILs を高分子化した形態の最も有利な R N R' R R X N N R R' X N R R" R' X R P R' R R X Imidazolium Pyridinium Ammonium Phosphonium Cation structures Anion structures BF4- PF6- NO3 -Cl- Br- CF 3 S O O O F3CO2S SO2CF3 N NCNCN 図1. イオン液体中の典型的なカチオンとアニオンの構造
重合性イオン液体:
光機能性高分子イオン液体材料への展開
鹿児島大学 大学院 理工学研究科 教授門川 淳一
1
はじめに
2
重合性イオン液体とポリ(イオン液体)
点は,実用的な材料としての応用のための加工性,柔軟性および耐久性の向上である。PILs 原料とし ての重合性 ILs は IL 構造のアニオンサイトあるいはカチオンサイトに重合基を導入することで得られ, これらのラジカル重合により対応する PILs を与える(スキーム 1)。前者の場合,通常の ILs のアニ オンを重合性アニオンにイオン交換することで得ることができる。後者の場合,重合基として典型的 なものはビニル,(メタ)アクリロイル,ビニルベンジル基であり,カチオンサイトに共有結合で導入 される。1- ビニルイミダゾールは市販の試薬であることから,様々なハロゲン化アルキルとの四級化 反応により簡便に 1- ビニルイミダゾリウム型の重合性 ILs を得ることができる。市販の試薬として購 N N R X n N HN R' R N HN R' R n Radical polymerization (a) (b) Polymerizable groups = O O O O CH2 Radical polymerization N N R X N N R N N R Cl Cl Br O O N N Br R O O N N R (a) (b) m m Br OH m + Cl O R = alkyl, vinyl スキーム1. アニオンサイト(a)およびカチオンサイト(b)に重合基を有する重合性ILsの重合 スキーム2. ビニルベンジル基(a)および (メタ)アクリラート基(b)を有する重合性ILsの典型的な合成手法 Radical polymerization
Cross-linked insoluble PIL N N X O O N N X O O n m スキーム3. 二つの重合基を有する重合性ILの重合
入できる塩化ビニルベンジル(スキーム 2(a)),あるいは臭化アルカノールと塩化(メタ)アクリロイ ルとの反応で得られる臭化アルキル(メタ)アクリラート(スキーム 2(b))と 1- アルキルイミダゾー ルとの反応では対応する重合性 ILs を与える5)。さらに 1- ビニルイミダゾールを用いた反応では重合 基を二つ有する重合性 ILs を得ることができる(スキーム 3)。このタイプの ILs はラジカル重合によ り架橋構造を有する不溶性で安定な PILs に変換可能であるため,実用的材料中のコンポーネント原料 としての高いポテンシャルを有すると考えられる。また,対応する塩を用いた重合性 ILs のアニオン 交換によっても望みのアニオンを導入できる。 PILs を調製する主な目的の一つは,バッテリーや燃料セル中での電解質としての可能性を評価する ことである6)。例えば,大野らは,イミダゾリウム型重合性イオン液体のラジカル重合により,高い イオン伝導度を有する柔軟なフィルムが得られることを報告している7)。最近,著者は,適当な重合 性 ILs のラジカル重合を利用したセルロース ‐ PIL コンポジット材料の創製を報告してきた8)。この 手法では,ある重合性 ILs がセルロースの膨潤により結晶構造を部分的に崩壊させる能力を有してい ることが見いだされていることから,セルロースをこのような ILs に浸漬させて膨潤し,このシステ ム中での in-situ 重合を行うことで,目的のコンポジット材料が得られる。さらに,この手法は他の多 糖にも応用され,対応するコンポジット材料が得られている9)。 他のユニークで特異的な ILs の性質として,エネルギー的に異なった集積構造の存在によりイミダ ゾリウム型 ILs が励起波長依存性蛍光発光を示すことが報告されている10)。著者は,そのような ILs が新しい光機能性材料開発のためにふさわしいコンポーネントとなりうると考えた。そこで,ユニー クな蛍光特性を有する実用的 IL 材料の創製のため,まず,二種類の重合性 ILs,すなわち塩化 1- メチ ル-3-(4-ビニルベンジル) イミダゾリウム(1)と臭化 1-(3-メタクリロイルオキシ) プロピル-3-ビニル イミダゾリウム(2)のラジカル共重合による透明な PIL フィルムの創製が試みられた(図 2(a));前 者はポリスチレン主鎖を持つ PIL を与え,後者は二つの重合基の存在により架橋剤として機能する11)。 これらの重合性 ILs は,スキーム 2 に示したように 1-メチルイミダゾールあるいは 1-ビニルイミダ ゾールから,対応するハロゲン化アルキル誘導体による四級化により合成されている。フィルム状の
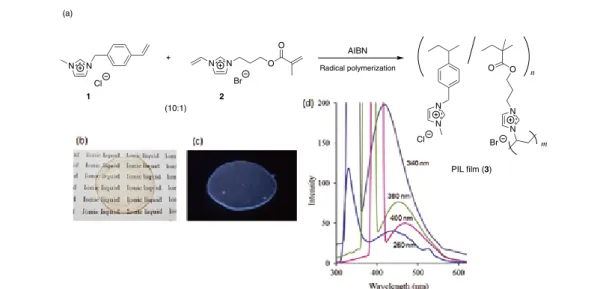
図2. AIBNを用いた1と2のラジカル共重合によるPILフィルム3の創製(a),PILフィルム3の写真(b),365nmのUV
光照射下での写真(c),および260-400nmでの励起によるPILフィルム3の蛍光スペクトル(d)
3
光機能性ポリ(イオン液体)材料の開発
(a) N N Cl N N Br O O 1 2 (10:1) AIBN Radical polymerization N Cl N N Br N O O n m PIL film (3)PIL(3)を得るために,1 と 2(10:1)およびラジカル開始剤 AIBN のメタノール溶液をガラス板に挟 み,この状態のまま 65℃で 30 分,さらに 75℃で 2 時間加熱し,重合とメタノールの留去を同時に行っ た。得られた架橋型 PIL(3)は図 2(b) および (c) に示したように透明なフィルム状であり,365 nm の UV 光照射によって青色の発光を示した。得られたフィルムは塩化 1-ブチル-3-メチルイミダゾリウ ム(BMIMCl)のような一般的なイミダゾリウム型 IL と同様な励起波長依存性発光特性を示した(図 2(d))。 著者は,代表的な赤色色素であるローダミン 6G の BMIMCl 溶液中において,広い波長領域での励 起によって,BMIMCl(ドナー)からローダミン 6G(アクセプター)への蛍光共鳴エネルギー移動 (FRET)12)が起こることを見出している13)。なぜなら,それぞれの励起波長による励起波長依存性発 光領域がローダミン 6G の吸収スペクトル領域と重なっているからである。それゆえに,その溶液中 での広い波長領域での励起により,ローダミン 6G 由来の発光が観測された。この結果を基盤として, 著者は,三原色の組み合わせにより多色発光可能な PIL フィルムをデザインした14)。この目的のため に,赤色色素としてのローダミン以外に二種類の蛍光色素,すなわち,緑色色素の 7-(ジエチルアミノ) クマリン-3-カルボン酸(DEAC)と青色色素のピラニンを用いた。これらの色素を PIL フィルムに組 み込むために,以下の反応により,メタクリラート基を有する重合性ローダミン,DEAC およびピラ ニン誘導体(4-6)を合成した。縮合剤を用いるローダミン B と 2-ヒドロキシエチルメタクリラート との直接縮合により重合性ローダミン誘導体 4 が得られた(スキーム 4)。また,文献記載の方法によ り,重合性 DEAC 誘導体 5 は塩化 DEAC と 2-ヒドロキシエチルメタクリラートから合成した(スキー ム 5)15)。さらに,ピラニンと塩化メタクリロイルの反応により重合性ピラニン誘導体 6 を合成した(ス キーム 6)。 次に,1,2 および 4,5 あるいは 6 とのラジカル共重合を行い,それぞれの色素を含有した PIL フィ ルム 7,8,9 を合成した(図 3(a))。得られたフィルムの蛍光スペクトルは広い励起波長領域(260 ‐ C O O OH Rhodamine B 2-Hydroxyethyl methacrylate + DCC / DMAP (condensing agent) 1,2-Dichloroethane DCC = DMAP = N N N N 4 O N N O O Cl O O O N N OH O Cl HO O O O N O Cl O O N O O O O O DEAC chloride + 2-Hydroxyethyl methacrylate Pyridine 5 スキーム4. 重合性ローダミン誘導体4の合成 スキーム5. 重合性DEAC誘導体5 の合成 SO3Na OH SO3Na NaO3S + Cl O Triethylamine DMF SO3Na O SO3Na NaO3S O Pyranine Methacryloyl chloride 6 スキーム6. 重合性ピラニン誘導体6の合成
400 nm)でそれぞれの色素の発光を示した。上記の PIL フィルム 3 の蛍光発光がフィルム 7-9 の吸収 波長と部分的に重なっていることから,260 ‐ 400 nm での励起によるこれらのフィルムの発光は,色 素部位の直接発光あるいはユニット1と2の色素部位へのFRETのいずれかによると考えられる。実際, これらのフィルム 7-9 は 365 nm の光照射により,それぞれ赤,緑,青色の発光を示した(図 3(b))。 上記の赤,緑,青色色素の可能な組み合わせを利用して,望みの発光色を呈する PIL フィルムが合 成された。AIBN を用いて,色素の三種類の組み合わせ(4+5,4+6,5+6)と 1 および 2 を共重合さ せて PIL フィルム 10-12 を得た(図 3(a))。得られたフィルムの蛍光スペクトルは,260 ‐ 400 nm で の励起において導入した色素に由来するそれぞれ二種類の発光を示した。この結果は,フィルム中に おいてそれぞれの色素が直接あるいは FRET によって個別に発光したことを示している。さらに,三 つの重合性色素と 1 および 2 の共重合により,三種類の色素部位を有する PIL フィルム 13 も合成した。 このフィルムの蛍光スペクトルは,260 ‐ 400 nm での励起においてそれぞれの色素に由来する三種類 の発光を示した。複数の色素を含有した上記の PIL フィルムは,一つの波長での励起により,色素の 組み合わせに依存した黄,マゼンタ,シアン,白の蛍光発光を示した(図 3(b))。 本稿において,著者は重合性 ILs のラジカル重合による機能性 PILs の創製について概説した。望み の重合性 ILs は簡便な反応経路により合成された。特に,それらの共重合により,通常の ILs と同様 にユニークで特異的な光機能を示す PILs が効率的に得られた。今後,新規な重合性 ILs がデザイン・ 合成され,その重合により,更なる高機能な PIL 材料へと展開されるであろう。
Polymerizable fluorescent dyes
Red Green Blue Yellow Magenta White
PIL film 7
Cyan
PIL film 8 PIL film 9 PIL film 10 PIL film 11 PIL film 12 PIL film 13 (b) (a) N N Cl N N Br O O 1 2 AIBN N Cl N N Br N O O n m O O
Polymerizable fluorescent dyes (4 - 6)
Unit 1
Unit 2 O O
Fluorescent dye unit
PIL filmes carring unit 4; 7 unit 5; 8 unit 6; 9 unit 4 + 5; 10 unit 4 + 6; 11 unit 5 + 6; 12 unit 4 + 5 + 6; 13 Fluorescent dye Fluorescent dye 図3. 1,2および重合性蛍光色素のラジカル共重合による様々な組み合わせの色素部位を有するPILフィルムの 合成(a)および365nmの光照射による多色発光(b)
4
おわりに
謝辞
著者は,文献に共著者として記載された共同研究者の献身的な協力に深謝するものである。
文献
1) T. Welton, Chem. Rev. 1999, 99, 2071; J. S. Wilkes, Green Chem. 2002, 4, 73; T. Erdmenger, C. Guerrero-Sanchez,
J. Vitz, R. Hoogenboom, U. S. Schubert, Chem. Soc. Rev. 2010, 39, 3317.
2) J. H. Davis, Chem. Lett. 2004, 33, 1072; S. G. Lee, Chem. Commun. 2006, 1049; R. Giernoth, Angew. Chem. Int. Ed. 2010, 49, 2834.
3) O. A. E. Seoud, A. Koschella, L. C. Fidale, S. Dorn, T. Heinze, Biomacromolecules 2007, 8, 2629; M. E.
Zakrzewska, E. B. Lukasik, R. B. Lukasik, Energy & Fuels 2010, 24, 737.
4) O. Green, S. Grubjesic, S. Lee, M. A. Firestone, J. Macromol. Sci.: Part C: Polym. Rev. 2009, 49, 339; D.
Mecerreyes, Prog. Polym. Sci. 2011, 36, 1629; J. Yuan, D. Mecerreyes, M. Antonietti, Prog. Polym. Sci. 2013, 38,
1009.
5) T. Fukushima, A. Kosaka, Y. Ishimura, T. Yamamoto, T. Takigawa, N. Ishii, T. Aida, Science 2003, 300, 2072; J.
Tang,H. Tang, W. Sun, M. Radosz, Y. Shen, J. Polym. Sci. Polym. Chem. 2005, 43, 5477; J. Tang, H. Tang, W.
Sun, M. Radosz, Y. Shen, Polymer 2005, 46, 12460.
6) H. Ohno, Electrochim. Acta 2001, 46, 1407; M. Yoshizawa, W. Ogihara, H. Ohno, Polym. Adv. Technol. 2002, 13,
589; H. Ohno, M. Yoshizawa, W. Ogihara, Electrochim. Acta 2004, 50, 255.
7) S. Washiro, M. Yoshizawa, H. Nakajima, H. Ohno, Polymer 2004, 45, 1577.
8) M. Murakami, Y. Kaneko, J. Kadokawa, Carbohydr. Polym. 2007, 69, 378; J. Kadokawa, M. Murakami, Y.
Kaneko, Compos. Sci. Technol. 2008, 68, 493; A. Takegawa, M. Murakami, Y. Kaneko, J. Kadokawa, Polym. Compos. 2009, 30, 1837; K. Prasad, S. Mine, Y. Kaneko, J. Kadokawa, Polym. Bull. 2010, 64, 341; J. Kadokawa,
in Ionic Liquids, Application and Perspectives, ed. by A. Kokorin, InTech, Rijeka, 2011, pp. 95–114; J. Kadokawa, J. Biobased Mater. Bioenergy 2013, 7, 3.
9) K. Prasad, J. Kadokawa, Polym. Compos. 2010, 31, 799; J. Kadokawa, T. Kato, M. Setoyama, K. Yamamoto, J. Polym. Environ. 2013, 21, 512.
10) A. Paul, P. K. Mandal, A. Samanta, Chem. Phys. Lett. 2005, 402, 375; A. Paul, P. K. Mandal, A. Samanta, J. Phys. Chem. B 2005, 109, 9148; P. K. Mandal, A. Paul, A. Samanta, J. Photochem. Photobiol. A: Chem. 2006, 182, 113; A.
Paul, A. Samanta, J. Chem. Sci. 2006, 118, 335.
11) S. Wakizono, K. Yamamoto, J. Kadokawa, J. Photochem. Photobiol. A: Chem. 2011, 222, 283.
12) A. Miyawaki, J. Llopis, R. Heim, J. M. McCaffery, J. A. Adams, M. Ikura, R. Y. Tsien, Nature 1997, 388, 882; J. R.
Lakowicz, in Principle of Fluorescence Spectroscopy 2nd Edn., Plenum, New York, 1999.
13) H. Izawa, S. Wakizono, J. Kadokawa, Chem. Commun. 2010, 46, 6359.
14) S. Wakizono, K. Yamamoto, J. Kadokawa, J. Mater. Chem. 2012, 22, 10619; J. Kadokawa, in Ionic Liquids, New Aspects for the Future, ed. by J. Kadokawa, InTech, Rijeka, 2013, pp. 653–672.
15) St pie , D. Bogdał, Czasopismo Techniczne. Chemia 2004, 101, 141; D. Bogdał, I. St pie , J. Santera, E. Gondek, Polimery 2003, 48, 111. 執筆者紹介